严格控制微生物是医疗器械产品(特别是无源产品)研发、生产阶段的重要质控要求,微生物控制在医疗器械质量要求中占据了重要位置,也是反映医疗器械生产质控体系的重要参数。大部分与人体接触的医疗器械产品均需进行微生物限度检测。
服务范围
※微生物限度
※初始污染菌检查
※ 无菌检查
※细菌内毒素检测
※生物负载
※杀菌剂功效评估
※抑菌实验
方法依据
微生物限度 |
中国药典、美国药典、欧洲药典、GB 15979、GB/T 19973、ISO 11737 |
无菌检查 |
中国药典、美国药典、欧洲药典、ISO 11737 |
内毒素测定 |
中国药典、美国药典、欧洲药典、YY/T 0616、GB/T 14233.2 |
生物负载 |
ISO 11737-1 |
杀菌剂功效评估 |
美国药典、GB 15979、消毒技术规范 |
抑菌试验 |
美国药典、GB 15979、消毒技术规范 |
服务流程
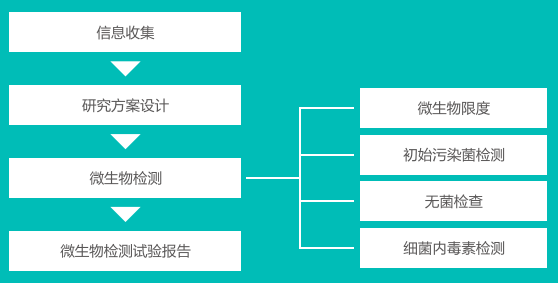
我们的服务优势
瑞旭集团(CIRS)创立于2007年,是一家专业的产品合规技术咨询服务机构,总部位于中国杭州,在爱尔兰、美国、英国、韩国及中国北京、南京等地设立分支机构,技术服务涵盖化学、材料、医疗器械、诊断试剂、化妆品、食品及保健品、消毒品等领域。 在医疗器械领域,瑞旭集团提供医疗器械研发技术支持、安全性评价与检测、注册及备案、临床研究、质量管理体系辅导、生产许可、产品上市后合规管理等全产业链技术服务。

相关服务:

